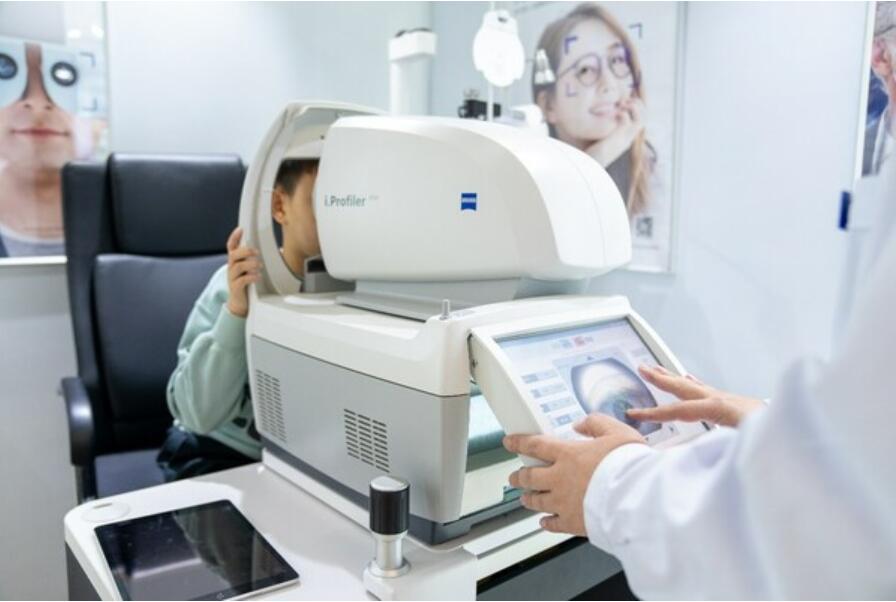
世界卫生创新峰会宣布 2024 年活动日期并与世界卫生组织建立战略合作伙伴关系
卡塔尔多哈2023年12月7日/美通社/ -- 由卡塔尔教育、科学与社会发展基金会 (QF) 发起的世界卫生创新峰会 (WISH) 宣布,WISH 2024 将于 2024 年 11 月 13 日和 14 日在多哈举行。 Dr Tedros Adhanom Ghebreyesus (seated left) , Director General, WHO, and Sultana Afdhal, CEO, WISH, sign a collaboration agreement at Qatar Foundation’s headquarters, witnessed by Her Excellency Dr Hanan Mohamed Al Kuwari (top right), Minister of Public Health in Qatar, and representatives of WHO.在为期两天的会议中,将有 2,000 多名卫生政策制定者、创新者、研究人员和从业人员齐聚卡塔尔,为世界上最重大的一些卫生难题寻求创新型解决方案。WISH 2024 将是 WISH 的第七届会议——其已在全球卫生日程中牢固确立为一项重要活动。经 QF 主席Sheikha Mozabint Nasser 殿下与世界卫生组织 (WHO) 总干事Tedros Adhanom Ghebreyesus博士进行高层讨论后,WISH 将在 WISH 2024 前与 WHO 建立战略合作伙伴关系,并将双方近年来持续的关系正式化。本次合作伙伴关系将以 WHO 领导的三个合作研究项目为核心,生成循证调查报告,供活动期间深入讨论。此外,地方和国际上的合作伙伴将与 WISH 一道,编写卫生系统、伦理、生理和心理健康等一系列问题的专题报告,供大家在峰会上讨论。WISH 2024 将继续强调从区域视角看待全球健康问题的必要性。12 月 4 日,WISH 首席执行官 Sultana Afdhal 与 Tedros 博士一起出席了 WISH 与 WHO 签署合作协议的仪式。卡塔尔公共卫生部长、现任世界卫生组织执行委员会主席Hanan Mohamed Al Kuwari阁下(博士)见证了这份协议的签署。卡塔尔公共卫生部是 WISH 的战略合作伙伴,从十年前第一届峰会开始,就为其提供了源源不断的支持。Sultana Afdhal 表示:"我们很荣幸能向大家宣布,明年 11 月我们将继续迎来 WISH 2024;我们仍然将致力于搭建一个平台,通过循证研究为全球卫生实践提供参考。Tedros 博士来参加 WISH 2024 启动仪式是我们莫大的荣幸,他将与我们分享关于战略合作伙伴关系的最新消息,共同展望我们对建设一个更健康、更公平的世界的愿景。"Tedros 博士表达了他对卡塔尔基金会主席Sheikha Mozabint Nasser 殿下的感激,对于新合作伙伴关系的赞赏,他说:"在我们获得了巨大影响的基础上,我们扩大了与 WISH 的合作关系,这将进一步证明,我们有决心共同应对全球紧迫的卫生问题,这些问题包括结核病、姑息治疗和在武装冲突中保护健康。我们期待能为证据基础做出贡献,并为双方合作做出更加切实的努力。"
-
2023-12-11 17:46